Реакція естерифікації — це захоплюючий хімічний процес, який об’єднує кислоти й спирти, створюючи естери — сполуки, що надають фруктам їхній аромат, а нашому життю — безліч корисних продуктів. Уявіть: молекули, наче партнери на танцполі, зливаються в елегантному хімічному танці, щоб народити щось нове й унікальне. У цій статті ми розберемо, як саме відбувається ця реакція, які умови потрібні, які продукти вона дає та як застосовується в реальному світі.
Що таке реакція естерифікації?
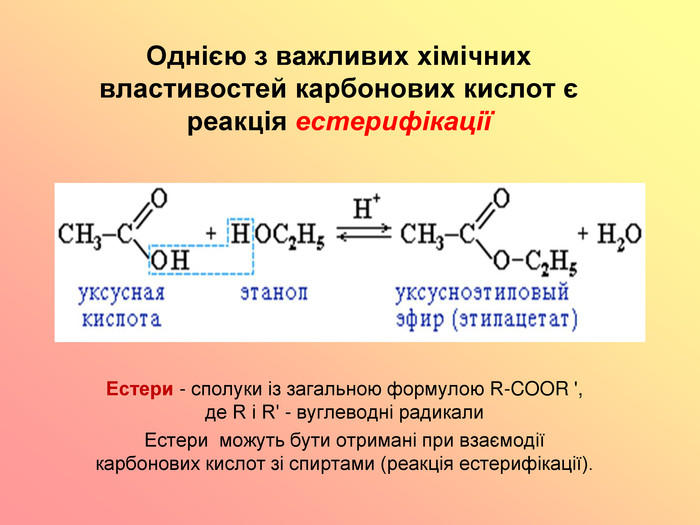
Реакція естерифікації — це процес взаємодії карбонової кислоти зі спиртом за наявності каталізатора, найчастіше кислотного, що призводить до утворення естеру та води. Це класична реакція органічної хімії, яка належить до конденсаційних реакцій, адже дві молекули об’єднуються, “виштовхуючи” молекулу води. Уявіть, що кислота й спирт — це інгредієнти, які, змішуючись, створюють ароматний “коктейль” у вигляді естеру.
Основна формула реакції виглядає так:
RCOOH + R’OH ⇌ RCOOR’ + H₂O
Тут RCOOH — карбонова кислота, R’OH — спирт, RCOOR’ — естер, а H₂O — вода. Зверніть увагу на знак “⇌”: реакція оборотна, і це ключова особливість, про яку ми поговоримо далі.
Механізм реакції: як це працює на молекулярному рівні?
Щоб зрозуміти, як саме відбувається естерифікація, давайте зазирнемо в молекулярний світ. Реакція проходить у кілька етапів, і кожен із них — як окремий крок у складному танці. Ось як це виглядає:
- Протонизація карбонової кислоти. Каталізатор (зазвичай сірчана кислота, H₂SO₄) додає протон (H⁺) до карбоксильної групи кислоти, роблячи її більш реактивною. Це наче “зарядження” молекули енергією для подальшої взаємодії.
- Нуклеофільна атака спирту. Спирт, маючи вільну пару електронів на атомі кисню, атакує позитивно заряджений вуглець карбоксильної групи. Це створює нестійкий проміжний продукт — тетраедричний інтермедіат.
- Усунення води. Проміжний продукт втрачає молекулу води, що дозволяє сформуватися зв’язку між кислотою та спиртом, утворюючи естер.
- Депротонизація. Каталізатор забирає протон назад, стабілізуючи кінцевий продукт — естер.
Цей механізм звучить складно, але уявіть собі конструктор: молекули кислоти й спирту з’єднуються, відкидаючи “зайву” воду, щоб створити нову, більш складну структуру. Каталізатор тут — як інструкція, що прискорює процес.
Умови для реакції естерифікації
Щоб реакція естерифікації відбулася, потрібні певні умови. Без них молекули не “затанцюють”. Ось ключові фактори:
- Наявність каталізатора. Найчастіше це концентрована сірчана кислота, яка прискорює реакцію, знижуючи енергію активації. У деяких випадках використовують хлоридну кислоту або спеціальні ферменти (у біохімії).
- Температура. Реакцію зазвичай проводять за нагрівання (50–100°C), щоб прискорити процес, але не перегрівають, щоб уникнути розкладання реагентів.
- Надлишок реагентів. Оскільки реакція оборотна, надлишок спирту або кислоти зміщує рівновагу в бік утворення естеру (за принципом Ле Шательє).
- Видалення води. Воду, що утворюється, часто видаляють (наприклад, за допомогою дегідратаційних агентів або дистиляції), щоб запобігти зворотній реакції.
Ці умови — як ідеальний рецепт: якщо все зробити правильно, естер вийде чистим і в хорошій кількості. Наприклад, у лабораторії для видалення води часто використовують азеотропну дистиляцію, додаючи бензол або толуол.
Типи естерифікації: не лише кислота + спирт
Хоча класична естерифікація передбачає взаємодію карбонової кислоти зі спиртом, є й інші її різновиди. Кожен із них має свої особливості та застосування:
- Кислотно-каталізована естерифікація. Найпоширеніший тип, описаний вище, із використанням кислотного каталізатора.
- Ферментативна естерифікація. У біохімії ферменти, такі як ліпази, каталізують утворення естерів. Цей метод екологічніший і використовується в косметичній та харчовій промисловості.
- Трансестерифікація. Це реакція між естером і спиртом, де один естер перетворюється на інший. Наприклад, її використовують для виробництва біодизеля.
- Естерифікація ангідридів кислот. Ангідриди кислот реагують зі спиртами без каталізатора, утворюючи естери. Цей метод швидший, але дорожчий.
Кожен тип естерифікації відкриває нові можливості. Наприклад, трансестерифікація — ключ до створення екологічно чистого палива, а ферментативна естерифікація дозволяє створювати натуральні ароматизатори без агресивних хімікатів.
Продукти естерифікації: що ми отримуємо?
Головний продукт естерифікації — естер — це сполука з унікальними властивостями. Естери мають приємний запах, нагадуючи фрукти чи квіти, і широко застосовуються в різних галузях. Ось кілька прикладів:
| Естер | Кислота | Спирт | Запах/Застосування |
|---|---|---|---|
| Етил ацетат | Оцтова кислота | Етанол | Фруктовий, використовується в лаках і парфумах |
| Метил саліцилат | Саліцилова кислота | Метанол | М’ятний, у мазях і ароматизаторах |
| Ізоаміл ацетат | Оцтова кислота | Ізоаміловий спирт | Банановий, у кондитерських виробах |
Джерело даних: навчальні посібники з органічної хімії, chem.libretexts.org.
Окрім естерів, утворюється вода, яка може впливати на хід реакції, якщо її не видаляти. У промислових масштабах воду відганяють, щоб максимізувати вихід естеру.
Застосування естерифікації в реальному світі
Естерифікація — це не просто лабораторний експеримент, а процес, який змінює наше життя. Ось як естери використовуються в різних галузях:
- Харчова промисловість. Естери створюють аромати для цукерок, напоїв і десертів. Наприклад, ізоаміл ацетат імітує банановий смак у жуйках.
- Парфумерія. Більшість парфумів містять естери, які надають їм квіткові чи фруктові ноти.
- Фармацевтика. Естери, як-от аспірин (ацетилсаліциловий естер), використовуються в ліках.
- Промисловість. Естери застосовують у виробництві пластмас, розчинників і біодизеля.
Цікаво, що естери також відіграють роль у природі. Наприклад, вони є частиною феромонів комах і ароматичних сполук у фруктах, які приваблюють тварин для поширення насіння.
Цікаві факти про естерифікацію
Цікаві факти
🌱 Естери в природі. Банани, ананаси та полуниця пахнуть так апетитно завдяки естерам, які синтезуються в їхніх клітинах природним шляхом.
⭐ Перший синтез естеру. Реакцію естерифікації вперше описали в XIX столітті, а сам термін “естер” походить від німецького “Essigäther” (оцтовий ефір).
🔬 Естери в космосі. У 2009 році астрономи виявили етилформіат — естер із запахом малини — у міжзоряних хмарах!
🧪 Екологічний потенціал. Трансестерифікація рослинних олій допомагає створювати біодизель, зменшуючи залежність від викопного палива.
Практичні поради для лабораторної естерифікації
Якщо ви студент або хімік-початківець, ось кілька порад, як провести естерифікацію в лабораторії:
- Використовуйте надлишок спирту. Це недорогий спосіб змістити рівновагу реакції в бік утворення естеру.
- Контролюйте температуру. Перегрів може призвести до побічних реакцій, як-от дегідратація спирту.
- Дотримуйтесь техніки безпеки. Сірчана кислота агресивна, тож використовуйте рукавички й окуляри.
- Перевірте чистоту продукту. Після реакції естер потрібно очистити дистиляцією або екстракцією.
Ці поради допоможуть вам отримати чистий естер із приємним запахом і високим виходом. Наприклад, синтез етил ацетату в лабораторії — це класичний експеримент, який демонструє основи органічної хімії.
Чому естерифікація важлива?
Естерифікація — це не просто хімічна реакція, а місток між наукою та повсякденним життям. Вона дозволяє створювати продукти, які роблять наше життя смачнішим, пахучішим і зручнішим. Від ароматів улюбленого парфуму до екологічного палива — естери всюди. А ще ця реакція вчить нас, як молекули можуть співпрацювати, створюючи щось нове, наче команда, що працює над великим проєктом.
Розуміння естерифікації відкриває двері до світу органічної хімії, де кожна молекула має свою історію.
Наступного разу, коли ви відчуєте аромат фруктів чи намажете крем із приємним запахом, згадайте: це все — магія естерифікації, яка відбувається завдяки взаємодії простих, але дивовижних молекул.