Уявіть, що ви відкриваєте двері до невидимого світу, де молекули розпадаються на заряджені частинки, створюючи електричний танець у розчинах. Цей процес, відомий як розпад електроліту на йони, є основою багатьох природних і технологічних явищ. Від роботи акумуляторів до підтримання життя в наших клітинах – іонізація електролітів відіграє ключову роль. У цій статті ми розберемо кожен аспект цього захопливого явища, пояснимо складне простими словами та додамо цікавих деталей, щоб ви відчули себе справжніми хіміками.
Що таке електроліти та чому вони розпадаються?
Електроліти – це речовини, які в розчині або розплаві розпадаються на йони, забезпечуючи електропровідність. Уявіть їх як провідників, що дозволяють електричному струму текти через рідину, подібно до мосту, що з’єднує два береги річки. Солі, кислоти та основи – найпоширеніші приклади електролітів. Але чому вони розпадаються? Все залежить від їхньої здатності утворювати заряджені частинки – йони – під впливом води чи іншої полярної рідини.
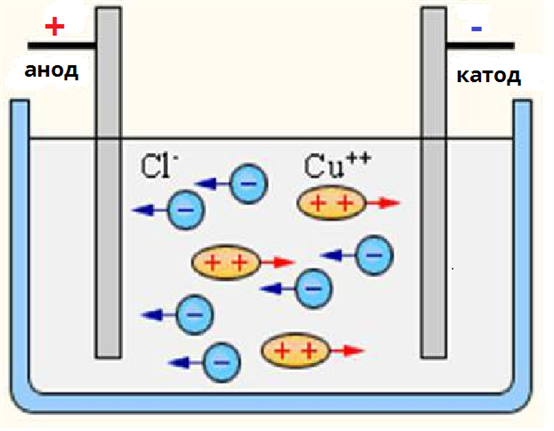
Коли електроліт, наприклад, кухонна сіль (NaCl), потрапляє у воду, молекули води, подібно до маленьких магнітів, оточують і “розтягують” йонну решітку. Позитивно заряджені йони натрію (Na⁺) і негативно заряджені йони хлору (Cl⁻) відриваються один від одного, стаючи вільними. Цей процес називається дисоціацією, і він є серцем електролітичного розпаду.
Типи електролітів: Сильні та слабкі
Не всі електроліти поводяться однаково. Їх можна поділити на дві великі групи: сильні та слабкі. Давайте розберемося, чим вони відрізняються.
- Сильні електроліти: Ці речовини повністю дисоціюють у розчині, утворюючи максимальну кількість йонів. Наприклад, хлорид натрію (NaCl) або сірчана кислота (H₂SO₄). Уявіть їх як вечірку, де всі гості активно танцюють, не залишаючи нікого осторонь.
- Слабкі електроліти: Вони дисоціюють лише частково, створюючи меншу кількість йонів. Оцтова кислота (CH₃COOH) – класичний приклад. Це як вечірка, де лише кілька гостей танцюють, а решта сидить біля стін.
Різниця між сильними та слабкими електролітами впливає на їхню електропровідність і хімічну активність. Сильні електроліти краще проводять струм, тоді як слабкі менш ефективні, але часто відіграють важливу роль у біологічних процесах.
Як відбувається процес дисоціації?
Процес розпаду електроліту на йони – це не просто хаотичне розщеплення. Це складний танець молекул, керований законами хімії та фізики. Давайте розберемо його покроково.
- Контакт із розчинником: Електроліт (наприклад, сіль) потрапляє у воду. Полярні молекули води починають взаємодіяти з йонами електроліту.
- Гідратація: Молекули води оточують йони, утворюючи гідратну оболонку. Позитивний кінець молекули води (атом водню) притягується до негативних йонів, а негативний (атом кисню) – до позитивних.
- Розрив зв’язків: Енергія взаємодії між водою та йонами перевищує силу йонних чи ковалентних зв’язків у молекулі електроліту, що призводить до їхнього розпаду.
- Утворення вільних йонів: Йони стають вільними, але не ізольованими – їх оточує гідратна оболонка, яка стабілізує їх у розчині.
Цей процес звучить просто, але він залежить від багатьох факторів: природи електроліту, температури, концентрації розчину та типу розчинника. Наприклад, у неполярних розчинниках, таких як бензол, електроліти зазвичай не дисоціюють, адже там немає “магнітів”, які б розтягували молекули.
Роль розчинника: Чому вода така особлива?
Вода – королева розчинників, і це не випадково. Її висока діелектрична проникність (близько 80) послаблює електростатичну взаємодію між йонами, полегшуючи їхній розпад. Крім того, молекули води мають дипольну структуру: один кінець молекули злегка позитивний, інший – злегка негативний. Це дозволяє воді ефективно “захоплювати” йони.
Цікаво, що не лише вода може бути розчинником. Наприклад, рідкий аміак або метанол також здатні підтримувати дисоціацію, хоча й менш ефективно. У біологічних системах, таких як клітини, вода залишається основним середовищем для йонних реакцій, забезпечуючи транспорт поживних речовин і сигналів.
Фактори, що впливають на дисоціацію
Процес розпаду електроліту на йони не є універсальним – він залежить від кількох ключових факторів. Розуміння цих факторів допомагає пояснити, чому одні розчини краще проводять електрику, ніж інші.
| Фактор | Опис | Приклад |
|---|---|---|
| Концентрація | При високій концентрації йони можуть взаємодіяти між собою, знижуючи ступінь дисоціації. | Розчин NaCl 0.1 М дисоціює краще, ніж 1 М. |
| Температура | Підвищення температури збільшує енергію молекул, сприяючи дисоціації. | Гаряча вода розчиняє сіль швидше. |
| Тип розчинника | Полярні розчинники (вода) сприяють дисоціації, неполярні – ні. | NaCl не дисоціює в бензолі. |
Джерело даних: Загальна хімія, підручники для ВНЗ.
Ці фактори не лише впливають на дисоціацію, але й визначають практичне застосування електролітів. Наприклад, у батареях використовують розчини з оптимальною концентрацією, щоб максимізувати електропровідність.
Практичне значення розпаду електролітів
Розпад електролітів на йони – це не просто хімічна цікавинка, а основа багатьох процесів у природі та технологіях. Давайте розглянемо кілька ключових сфер, де цей процес відіграє вирішальну роль.
- Біологія: У наших клітинах йони натрію, калію та кальцію забезпечують передачу нервових імпульсів і скорочення м’язів. Без дисоціації електролітів ми б не могли рухатися чи думати.
- Енергетика: У батареях і акумуляторах (наприклад, літій-іонних) йони рухаються між електродами, створюючи електричний струм.
- Промисловість: Електроліз, що базується на дисоціації, використовується для виробництва алюмінію, хлору та інших речовин.
- Медицина: Ізотонічні розчини (наприклад, фізіологічний розчин) підтримують баланс йонів у організмі під час інфузій.
Ці приклади показують, наскільки універсальним є процес дисоціації. Він буквально тримає світ у русі – від клітин нашого тіла до заводських цехів.
Цікаві факти про розпад електролітів
Ось кілька захопливих фактів про розпад електролітів, які здивують навіть досвідчених хіміків!
- 🌱 Вода в космосі: Навіть у мікрогравітації вода може сприяти дисоціації електролітів, що важливо для експериментів на МКС.
- ⚡ Електроліти в спорті: Спортивні напої містять електроліти (Na⁺, K⁺), які компенсують втрату йонів під час потовиділення.
- 🔬 Найслабший електроліт: Вода сама по собі є дуже слабким електролітом, адже лише 1 з 555 мільйонів молекул H₂O дисоціює на H⁺ і OH⁻.
- 🌍 Океан як електроліт: Морська вода – природний розчин електролітів, що проводить електрику, тому блискавки часто б’ють у море.
Ці факти показують, наскільки різноманітним і багатогранним є світ електролітів. Вони всюди – від нашого тіла до глибин океану!
Типові помилки під час вивчення дисоціації
Розпад електролітів здається простим, але навіть досвідчені студенти припускаються помилок. Ось кілька поширених пасток і як їх уникнути.
- Плутанина між дисоціацією та іонізацією: Дисоціація – це розпад уже наявних йонів, тоді як іонізація – утворення нових йонів із нейтральних молекул. Наприклад, NaCl дисоціює, а NH₃ іонізується у воді.
- Ігнорування слабких електролітів: Багато хто вважає, що всі електроліти повністю розпадаються. Слабкі електроліти, як оцтова кислота, цього не роблять, що впливає на їхню поведінку.
- Неправильне розуміння ролі розчинника: Деякі думають, що дисоціація можлива в будь-якому середовищі. Насправді потрібен полярний розчинник, як вода.
Розуміння цих нюансів допоможе вам уникнути плутанини та глибше осягнути тему. Якщо ви студент, зверніть увагу на ці моменти перед іспитом!
Як поглибити знання про електроліти?
Якщо ви хочете не просто зрозуміти, а й відчути магію розпаду електролітів, ось кілька практичних порад.
- Проведіть експеримент: Розчиніть сіль у воді та виміряйте електропровідність за допомогою простого тестера. Порівняйте з оцтом – різниця вас здивує!
- Вивчайте біологічні аспекти: Дізнайтесь, як йони впливають на роботу серця чи нервової системи. Це додасть темі практичного значення.
- Поглибте теорію: Ознайомтесь із константою дисоціації (K_d) для слабких електролітів – це ключ до розуміння їхньої поведінки.
Ці кроки допоможуть вам не лише засвоїти теорію, але й побачити, як електроліти працюють у реальному світі. Хімія – це не лише формули, а й захоплива історія про те, як влаштований наш світ.