Уявіть собі: маленька, невидима частинка, що лежить в основі всього, що нас оточує — від зірок до піщинки під ногами. Атом, цей мікроскопічний будівельний блок Всесвіту, століттями залишався загадкою. Але хто першим наважився зазирнути в його таємничу будову, створивши першу модель атома? Ця стаття — захоплива подорож у світ наукових відкриттів, де ми розкриємо, як людство крок за кроком розгадувало структуру атома, і відкриємо ім’я піонера, який заклав фундамент сучасної атомної теорії.
Витоки ідеї атома: від філософії до науки
Ще за сотні років до появи сучасних лабораторій і мікроскопів людський розум намагався осягнути природу матерії. У V столітті до н.е. давньогрецькі філософи Левкіпп і Демокріт висунули сміливу ідею: усе в світі складається з неподільних частинок, які вони назвали «атомами» (від грецького «atomos» — неподільний). Їхнє бачення було геніальним, але залишалося лише філософською здогадкою, адже експериментальних доказів тоді не існувало.
Минули століття, і в XIX столітті наука почала набувати сучасних рис. Джон Дальтон у 1803 році оживив ідею атомів, запропонувавши, що кожен хімічний елемент складається з унікальних атомів, які поєднуються у певних пропорціях. Його «більярдна» модель атома зображала їх як тверді, неподільні кульки. Проте Дальтон не пояснював внутрішню структуру атома — його модель була лише першим кроком до розуміння матерії.
Революція Томсона: перша модель атома
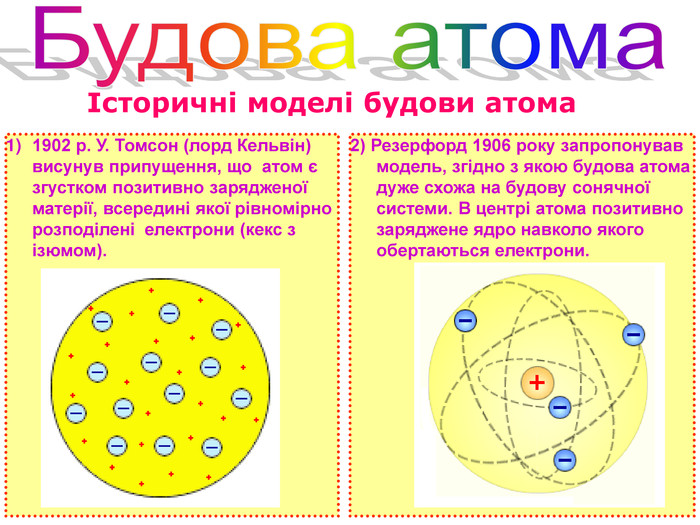
На межі XIX і XX століть наука зробила стрибок, який назавжди змінив наше уявлення про атом. У 1897 році англійський фізик Джозеф Джон Томсон, вивчаючи катодні промені, відкрив електрон — першу субатомну частинку з негативним зарядом. Це відкриття стало справжньою сенсацією, адже воно спростувало ідею про неподільність атома. Якщо в атомі є електрони, то як вони розташовані? Томсон узявся за це питання і в 1904 році запропонував першу модель будови атома, відому як «сливовий пудинг» (plum pudding model).
Модель Томсона уявляла атом як сферу позитивного заряду, в якій, ніби родзинки в пудингу, «вкраплені» негативно заряджені електрони. Позитивний заряд рівномірно розподілявся по всьому об’єму атома, забезпечуючи його електричну нейтральність. Ця модель була простою, але елегантною: вона пояснювала, чому атоми не мають загального заряду, адже позитивний заряд компенсував негативний заряд електронів.
Як Томсон дійшов до своєї моделі?
Відкриття електрона стало для Томсона ключем до розуміння будови атома. Він проводив експерименти з катодними променями — потоками частинок, що виникали в розріджених газах під дією електричного струму. Вимірюючи їхню швидкість і заряд, Томсон з’ясував, що ці частинки (які він назвав «корпускулами») набагато легші за атом водню. Це наштовхнуло його на думку, що електрони — складові атома.
Але як ці легкі частинки співіснують у нейтральному атомі? Томсон припустив, що позитивний заряд розподілений рівномірно, створюючи «хмару», в якій плавають електрони. Щоб уявити це, подумайте про желе з ягодами: желе — це позитивний заряд, а ягоди — електрони. Ця модель стала першим науковим поясненням внутрішньої структури атома, яке базувалося на експериментальних даних.
Чому модель Томсона була революційною?
Модель Томсона була проривом, адже вперше показала, що атом — не просто неподільна частинка, а складна система. Вона відкрила двері до нових досліджень і стала основою для подальших відкриттів. Томсон не лише висунув гіпотезу, а й підкріпив її експериментами, що зробило його модель науково обґрунтованою. Проте, як і будь-яка перша спроба, вона мала свої обмеження.
Недоліки моделі Томсона
Попри свою інноваційність, модель Томсона не могла пояснити всіх явищ. Ось ключові проблеми, які виявили вчені:
- Розсіювання частинок. Модель не могла пояснити, чому деякі частинки, наприклад альфа-частинки, відхиляються на великі кути при проходженні через речовину.
- Спектральні лінії. Атоми випромінюють світло певних довжин хвиль, створюючи унікальні спектри. Модель Томсона не пояснювала цього явища.
- Розташування електронів. Ідея рівномірного розподілу позитивного заряду не відповідала новим експериментальним даним про концентрацію маси в центрі атома.
Ці недоліки стали поштовхом для нових досліджень, які привели до наступного етапу в розвитку атомної теорії.
Експеримент Резерфорда: кінець ери «сливового пудингу»
У 1909 році учень Томсона, Ернест Резерфорд, разом із Гансом Гейгером і Ернестом Марсденом провів знаменитий експеримент із розсіювання альфа-частинок. Вони обстрілювали тонку золоту фольгу альфа-частинками (позитивно зарядженими ядрами гелію) і спостерігали, як ці частинки відхиляються. Результати шокували: більшість частинок проходили крізь фольгу без відхилення, але деякі відбивалися під великими кутами, а окремі навіть поверталися назад.
Цей експеримент показав, що атом не є однорідною «пудинговою» сферою, а має щільне, позитивно заряджене ядро, оточене електронами. У 1911 році Резерфорд запропонував планетарну модель атома, де майже вся маса зосереджена в крихітному ядрі, а електрони обертаються навколо нього, подібно до планет навколо Сонця.
Чим планетарна модель відрізнялася від моделі Томсона?
Для наочності порівняємо дві моделі в таблиці:
| Характеристика | Модель Томсона | Модель Резерфорда |
|---|---|---|
| Позитивний заряд | Рівномірно розподілений по всьому атому | Зосереджений у крихітному ядрі |
| Електрони | Вкраплені в позитивно заряджену сферу | Обертаються навколо ядра |
| Маса атома | Розподілена рівномірно | Зосереджена в ядрі |
| Експериментальна основа | Відкриття електрона | Розсіювання альфа-частинок |
Джерела даних: Вікіпедія, підручники з фізики.
Модель Резерфорда стала революційною, адже вона вперше показала, що атом переважно складається з порожнього простору, а його маса зосереджена в ядрі. Проте вона також мала недоліки, зокрема не пояснювала стабільність електронних орбіт.
Нільс Бор: квантовий стрибок у розумінні атома
У 1913 році датський фізик Нільс Бор удосконалив модель Резерфорда, додавши принципи квантової механіки. Він припустив, що електрони рухаються по чітко визначених орбітах і можуть «стрибати» між ними, випромінюючи або поглинаючи енергію у вигляді квантів. Ця модель пояснила атомні спектри і заклала основи сучасної квантової теорії.
Борівська модель стала мостом між класичною та квантовою фізикою, але вона все ще була спрощенням. Пізніше, у 1920-х роках, Вернер Гейзенберг і Ервін Шредінгер розвинули квантову механіку, яка замінила орбіти електронів на ймовірнісні «орбіталі» — хмари, де електрони найімовірніше перебувають.
Цікаві факти про перші моделі атома
Цікаві факти
- 🌟 Назва «електрон» не належить Томсону. Хоча Томсон відкрив електрон, термін «електрон» запропонував у 1891 році Джордж Джонстон Стоні для позначення «атома електрики».
- 🔬 Експеримент Резерфорда був випадковим. Резерфорд не очікував, що альфа-частинки відскакуватимуть від золотої фольги. Він назвав цей результат «неймовірним, як якби гарматне ядро відскочило від аркуша паперу».
- ⚛️ Модель Томсона надихнула мистецтво. Пудингова модель стала популярною метафорою в науковій поп-культурі, з’являючись у літературі та навіть кулінарних жартах!
- 📚 Томсон отримав Нобелівську премію. У 1906 році Джозеф Джон Томсон був удостоєний Нобелівської премії з фізики за дослідження електричних розрядів у газах, що привели до відкриття електрона.
Ці факти додають живості історії атомної теорії, показуючи, як наукові відкриття переплітаються з людською цікавістю та несподіваними поворотами.
Як перша модель атома вплинула на науку?
Модель Томсона стала відправною точкою для всіх подальших досліджень атомної структури. Вона не лише спростувала ідею неподільності атома, а й надихнула вчених шукати відповіді на нові питання. Завдяки Томсону Резерфорд провів свій експеримент, а Бор створив квантову модель. Цей ланцюжок відкриттів привів до сучасного розуміння атома, яке лежить в основі хімії, фізики та навіть нанотехнологій.
Сьогодні ми знаємо, що атом складається з ядра (протонів і нейтронів) і електронної хмари, яка описується квантовою механікою. Але без першого кроку Томсона — його сміливого припущення про «сливовий пудинг» — цей шлях міг би бути набагато довшим.
Чому варто знати про першу модель атома?
Розуміння історії атомної теорії — це не лише занурення в минуле, а й ключ до сучасних технологій. Від ядерної енергії до квантових комп’ютерів — усе почалося з питання, хто запропонував першу модель атома. Джозеф Джон Томсон, зі своєю пудинговою моделлю, став піонером, який відкрив двері до мікросвіту. Його внесок, хоч і був замінений досконалішими теоріями, назавжди залишиться першим променем світла в темряві невідомого.
Тож наступного разу, коли ви триматимете в руках будь-який предмет, згадайте: у його основі лежать атоми, таємницю яких почав розкривати Томсон. Ця історія — не просто наука, а захоплива пригода людського розуму, який прагне осягнути невидиме.