Уявіть собі величезний танцювальний майданчик, де атоми металів кружляють у гармонійному ритмі, а електрони, наче невловимі зірки, гасають між ними, створюючи міцний зв’язок. Це і є металевий зв’язок – унікальний тип хімічного зв’язку, який робить метали міцними, блискучими та провідними. У цій статті ми зануримося в глибини цього феномену, розкриємо його механізми, властивості та навіть поділимося цікавими фактами, які здивують і новачків, і просунутих читачів.
Що таке металевий зв’язок: основи для всіх
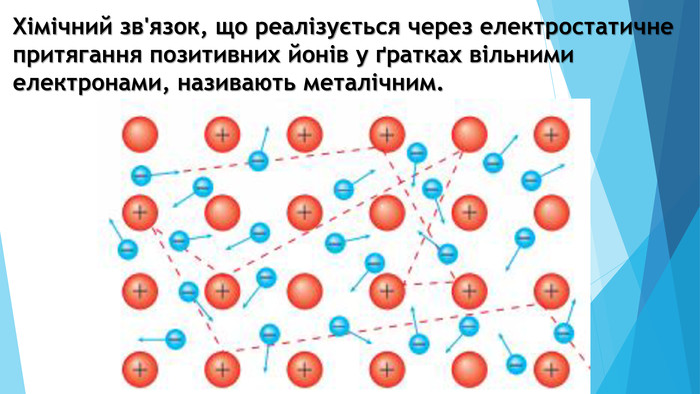
Металевий зв’язок – це хімічний зв’язок, який виникає між атомами металів завдяки делокалізованим електронам, що вільно рухаються в кристалічній структурі. Уявіть собі море електронів, у якому плавають позитивно заряджені іони металів. Ці електрони не прив’язані до конкретних атомів, а належать усій структурі, створюючи міцну взаємодію.
Чому це важливо? Саме металевий зв’язок визначає унікальні властивості металів: від їхньої здатності проводити електрику до пластичності, яка дозволяє кувати мечі чи створювати тонкі дроти. На відміну від інших типів зв’язків (ковалентного чи іонного), металевий зв’язок є гнучким і динамічним, що робить його особливим у світі хімії.
Як утворюється металевий зв’язок
Щоб зрозуміти, як працює металевий зв’язок, давайте розберемо цей процес покроково. Атоми металів мають особливість: у них мало валентних електронів (зазвичай 1–3), і вони легко віддають їх. Але замість того, щоб утворювати іонні чи ковалентні зв’язки, ці електрони стають делокалізованими, формуючи так званий «електронний газ».
Ось як це відбувається:
- Втрата електронів. Атоми металів віддають свої валентні електрони, перетворюючись на позитивно заряджені іони (катіони).
- Формування електронного моря. Віддані електрони не прив’язуються до конкретних атомів, а вільно рухаються по всій кристалічній гратці металу.
- Електростатична взаємодія. Позитивно заряджені іони притягуються до негативно зарядженого електронного «моря», що забезпечує міцність зв’язку.
Ця модель, відома як «теорія електронного газу», була запропонована ще на початку XX століття і досі є основою для розуміння металевого зв’язку. Але сучасна квантова хімія додає ще більше деталей, про які ми поговоримо далі.
Фізичні властивості металів: подарунок металевого зв’язку
Металевий зв’язок – це не просто абстрактна хімічна концепція. Він безпосередньо впливає на те, як метали поводяться у реальному світі. Ось ключові властивості, які ми завдячуємо цьому зв’язку:
- Електропровідність. Вільні електрони легко переносять електричний заряд, роблячи метали ідеальними провідниками. Наприклад, мідні дроти – основа електротехніки.
- Теплопровідність. Електрони також ефективно передають тепло, тому металеві каструлі швидко нагріваються.
- Пластичність і ковкість. Завдяки делокалізованим електронам атоми можуть зміщуватися без розриву зв’язку, що дозволяє кувати метали чи витягувати їх у тонкі листи.
- Металевий блиск. Електрони поглинають і відбивають світло, надаючи металам характерний блиск, як у срібла чи золота.
Ці властивості роблять метали незамінними в усьому – від будівництва мостів до створення ювелірних прикрас. Але чи всі метали однакові? Наприклад, ртуть у рідкому стані зберігає металевий зв’язок, але її властивості відрізняються від твердого заліза. Це показує, наскільки гнучким може бути цей тип зв’язку.
Порівняння металевого зв’язку з іншими типами
Щоб краще зрозуміти металевий зв’язок, порівняймо його з іншими типами хімічних зв’язків. Ось таблиця, яка допоможе розібратися:
| Тип зв’язку | Механізм | Приклади речовин | Властивості |
|---|---|---|---|
| Металевий | Делокалізовані електрони між катіонами | Мідь, залізо, золото | Електропровідність, пластичність, блиск |
| Ковалентний | Спільні електронні пари між атомами | Вода, діамант | Твердість, ізоляційні властивості |
| Іонний | Електростатичне притягання між іонами | Сіль (NaCl) | Крихкість, висока температура плавлення |
Джерела даних: Загальна хімія, підручник для ВНЗ; uk.wikipedia.org.
Ця таблиця показує, що металевий зв’язок унікальний своєю гнучкістю та універсальністю, що робить його незамінним для металів і їхніх сплавів.
Глибше в науку: квантова природа металевого зв’язку
Для просунутих читачів варто зануритися в квантову механіку, яка дає глибше розуміння металевого зв’язку. Уявіть електрони не просто як частинки, а як хвилі, що рухаються в кристалічній гратці. Ця модель, відома як зонна теорія, пояснює, чому метали такі ефективні провідники.
У металах валентні електрони займають так звані зони провідності – енергетичні рівні, де вони можуть вільно рухатися. Це відрізняє метали від діелектриків, у яких між валентною зоною та зоною провідності є велика енергетична щілина. Наприклад, у міді зона провідності заповнена делокалізованими електронами, що забезпечує її високу провідність.
Ця квантова природа пояснює, чому металевий зв’язок настільки міцний, але водночас дозволяє атомам зміщуватися, забезпечуючи пластичність.
Металевий зв’язок у сплавах
Металевий зв’язок не обмежується чистими металами. У сплавах, таких як сталь чи бронза, він також відіграє ключову роль. Сплави – це суміші різних металів або металів із неметалами, де металевий зв’язок адаптується до нової структури.
Наприклад, у сталі (сплав заліза з вуглецем) атоми вуглецю вбудовуються в кристалічну гратку заліза, змінюючи її властивості. Це робить сталь міцнішою, але менш пластичною, ніж чисте залізо. Така гнучкість металевого зв’язку дозволяє створювати матеріали з потрібними характеристиками для різних галузей – від будівництва до медицини.
Цікаві факти про металевий зв’язок
Металевий зв’язок – це не просто суха теорія, а справжнє диво природи! Ось кілька захопливих фактів, які відкриють його з нового боку:
- 🌟 Металевий водень. У 1935 році вчені передбачили існування металевого водню, де ковалентний зв’язок перетворюється на металевий під надвисоким тиском. У 2017 році Гарвардські вчені повідомили про його створення в лабораторії! (Джерело: журнал Science).
- ⚡ Суперпровідність. Деякі метали за наднизьких температур втрачають електричний опір завдяки особливостям металевого зв’язку. Це основа для створення надпотужних магнітів у МРТ.
- 🔩 Рідкі метали. Ртуть і галіум залишаються рідкими за кімнатної температури, але їхній металевий зв’язок зберігається, забезпечуючи провідність.
- 🛠️ Сплави в історії. Бронза (мідь із оловом) змінила хід цивілізації, адже металевий зв’язок у цьому сплаві забезпечував міцність знарядь праці.
Практичне значення металевого зв’язку
Металевий зв’язок має величезне значення в повсякденному житті. Без нього не було б сучасних технологій, транспорту чи навіть простих побутових речей. Ось кілька прикладів:
- Електроніка. Мідь і алюміній – основа для проводів і мікросхем завдяки своїй провідності.
- Будівництво. Сталь і титан використовуються для створення міцних конструкцій, від хмарочосів до мостів.
- Медицина. Титанові сплави застосовуються в протезах, адже вони міцні, легкі та біосумісні.
Цікаво, що металевий зв’язок навіть допомагає у космічних дослідженнях. Наприклад, алюмінієві сплави використовуються в корпусах супутників, адже вони легкі, але міцні.
Майбутнє металевого зв’язку: нові горизонти
Сучасна наука активно досліджує, як можна модифікувати металевий зв’язок для створення нових матеріалів. Наприклад, наноматеріали, такі як графен, мають елементи металевого зв’язку, що робить їх надпровідними. Уявіть майбутнє, де завдяки маніпуляціям із металевими зв’язками ми створюємо надлегкі, але міцні матеріали для космічних кораблів!
Металевий зв’язок – це ключ до інновацій, який уже зараз формує наше майбутнє.
Отже, металевий зв’язок – це не просто хімічна концепція, а справжній двигун прогресу. Від блискучих прикрас до космічних технологій, він пронизує наше життя, роблячи його зручнішим і цікавішим. Сподіваємося, ця стаття відкрила для вас нові грані цього дивовижного явища!