Уявіть собі атом як мініатюрну сонячну систему, де електрони гудуть навколо ядра, немов планети навколо зірки. Але замість чітких орбіт електрони живуть у хмароподібних зонах – орбіталях, кожна з яких має свою форму та енергію. Другий енергетичний рівень атома – це захоплюючий світ, де електрони знаходять свої “домівки”. У цій статті ми зануримося в деталі, розберемо, які орбіталі складають цей рівень, як вони влаштовані, і чому це важливо для хімії та фізики. Готові до подорожі в мікросвіт?
Що таке енергетичний рівень і чому другий особливий?
Енергетичні рівні – це “поверхи” в атомі, де електрони розташовуються залежно від їхньої енергії. Чим далі від ядра, тим вищий рівень і більша енергія. Другий енергетичний рівень (n=2) – це другий “поверх”, де електрони вже мають більше свободи, ніж на першому рівні, але ще не такі “розгульні”, як на вищих. Він особливий, бо тут з’являються нові типи орбіталей, які додають атомам різноманітності в хімічних реакціях.
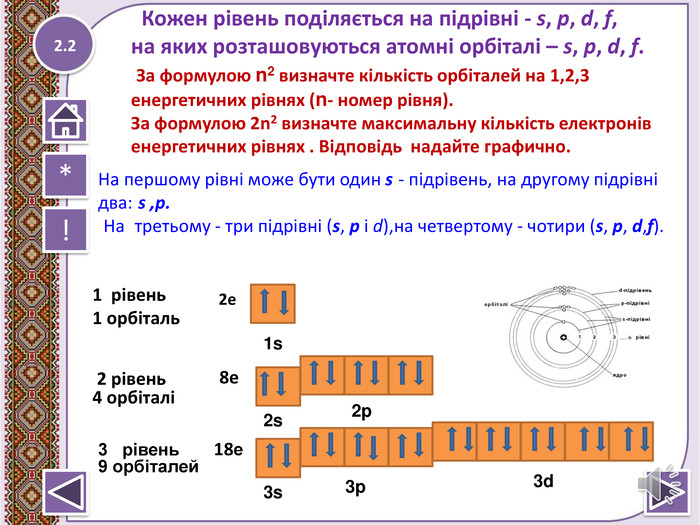
Другий рівень може вмістити до 8 електронів, що відповідає формулі 2n² (де n – номер рівня). Ці електрони розподіляються між орбіталями – спеціальними зонами, де ймовірність знайти електрон найвища. Але які саме орбіталі є на цьому рівні? Давайте розбиратися!
Орбіталі другого енергетичного рівня: повний склад
На другому енергетичному рівні є два типи орбіталей: s-орбіталь і p-орбіталі. Вони відрізняються формою, місткістю та роллю в атомі. Ось детальний розбір:
s-орбіталь: сферична основа
s-орбіталь – це як куляста хмара навколо ядра. Вона симетрична, і електрони в ній розподілені рівномірно в усіх напрямках. На другому рівні є одна s-орбіталь (2s), яка може вмістити 2 електрони.
- Форма: Сферична, нагадує м’яку пухнасту кулю.
- Місткість: 2 електрони (як і будь-яка орбіталь).
- Енергія: 2s-орбіталь має трохи вищу енергію, ніж 1s, але нижчу, ніж 2p.
- Роль: s-орбіталі часто беруть участь у формуванні хімічних зв’язків, наприклад, у молекулах водню чи метану.
s-орбіталь – це фундамент, з якого починається заповнення другого рівня. Вона проста, але незамінна, адже її електрони часто стають “будівельними цеглинками” для зв’язків.
p-орбіталі: гантелеподібна трійця
p-орбіталі – це більш складні структури, які з’являються на другому рівні. Вони мають форму гантелей або двох крапель, з’єднаних у центрі. На другому рівні є три p-орбіталі (2px, 2py, 2pz), кожна з яких орієнтована вздовж однієї з осей координат (x, y, z).
- Кількість: Три орбіталі (2px, 2py, 2pz).
- Форма: Гантелеподібна, з двома “лопатями” по різні боки ядра.
- Місткість: Кожна p-орбіталь вміщує 2 електрони, тож разом – 6 електронів.
- Енергія: p-орбіталі мають однакову енергію між собою, але вищу, ніж 2s.
- Роль: p-орбіталі ключові для утворення ковалентних зв’язків, особливо в органічних молекулах, як-от вуглець у метані чи кисень у воді.
Три p-орбіталі разом створюють своєрідну “квітку” навколо ядра, дозволяючи електронам займати різні просторові позиції. Це додає атомам гнучкості в хімічних реакціях.
Як електрони заповнюють другий рівень?
Електрони не просто “стрибають” на орбіталі – вони підкоряються чітким правилам. Ось як це відбувається:
- Принцип мінімальної енергії: Електрони спочатку заповнюють 2s-орбіталь, бо вона має нижчу енергію.
- Правило Гунда: У p-орбіталях електрони спочатку займають кожну орбіталь по одному (з однаковим спіном), а потім додаються другі електрони.
- Принцип Паулі: Кожна орбіталь може вмістити лише 2 електрони з протилежними спінами.
Наприклад, у атома кисню (8 електронів) перший рівень (1s) заповнюється 2 електронами, а на другому рівні 2s-орбіталь отримує 2 електрони, а решта 4 розподіляються між трьома 2p-орбіталями: по одному в 2px, 2py, 2pz, а четвертий додається до однієї з них.
| Елемент | Кількість електронів | Розподіл на 2-му рівні |
|---|---|---|
| Літій (Li) | 3 | 2s¹ |
| Берилій (Be) | 4 | 2s² |
| Кисень (O) | 8 | 2s² 2p⁴ |
| Неон (Ne) | 10 | 2s² 2p⁶ |
Дані таблиці базуються на електронних конфігураціях, опублікованих у підручниках з хімії, таких як Chemistry LibreTexts.
Чому другий рівень важливий для хімії?
Другий енергетичний рівень – це “серце” багатьох хімічних процесів. Електрони на 2s- і 2p-орбіталях часто є валентними, тобто беруть участь у формуванні зв’язків. Наприклад, у молекулі води (H₂O) кисень використовує свої 2p-електрони для створення ковалентних зв’язків із воднем. У вуглеці (C) 2s- і 2p-орбіталі беруть участь у гібридизації, формуючи міцні зв’язки в органічних молекулах.
Цей рівень визначає, як атоми взаємодіють один з одним, формуючи молекули, від простих, як вода, до складних, як ДНК.
Порівняння з іншими рівнями
Щоб зрозуміти унікальність другого рівня, порівняймо його з іншими:
- Перший рівень (n=1): Має лише одну 1s-орбіталь (2 електрони). Він простий, але обмежений.
- Третій рівень (n=3): Додаються d-орбіталі (3d), що вміщують до 10 електронів, але вони з’являються лише в перехідних металах.
Другий рівень – це “золота середина”, де з’являються p-орбіталі, але структура ще не ускладнена d- чи f-орбіталями. Це робить його ключовим для елементів 2-го періоду періодичної системи, таких як вуглець, азот і кисень.
Цікаві факти про другий енергетичний рівень
Другий енергетичний рівень ховає чимало сюрпризів! Ось кілька цікавих фактів, які розкривають його унікальність:
- 🌟 Основа життя: Вуглець, основа органічного життя, використовує 2s- і 2p-орбіталі для створення чотирьох зв’язків у молекулах, як-от метан чи білки.
- ⚡️ Неонова стабільність: Неон завершує другий рівень (2s² 2p⁶), що робить його інертним газом – він майже не реагує з іншими елементами!
- 🧬 Гібридизація: 2s- і 2p-орбіталі можуть “змішуватися”, утворюючи гібридні орбіталі (sp³, sp²), які формують геометрію молекул, як-от трикутна в борі чи тетраедрична в метані.
- 🔬 Квантова магія: p-орбіталі мають “вузол” у центрі (зона нульової ймовірності), що робить їх поведінку загадковою для квантової механіки.
Ці факти показують, як другий рівень поєднує простоту з дивовижною складністю, роблячи його ключовим для хімії та природи.
Практичне значення знань про другий рівень
Розуміння орбіталей другого рівня – це не просто академічна цікавість. Ці знання застосовуються в багатьох сферах:
- Хімія: Прогнозування реакційної здатності елементів.
- Матеріалознавство: Розробка нових матеріалів, як-от напівпровідники, де важливі p-орбіталі кремнію.
- Біологія: Розуміння структури біомолекул, таких як ДНК, де зв’язки формуються за участю 2p-орбіталей.
Навіть у повсякденному житті ці знання допомагають зрозуміти, чому вода рідка, а вуглекислий газ – газоподібний. Це все завдяки орбіталям другого рівня!
Знання про орбіталі другого рівня відкривають двері до розуміння того, як влаштований наш світ на мікроскопічному рівні.