Що таке карбонові кислоти: основи для розуміння
Карбонові кислоти – це органічні сполуки, які відіграють ключову роль у хімії, біології та навіть у нашому повсякденному житті. Уявіть їх як маленькі молекулярні “працівники”, які беруть участь у створенні запаху оцту, смаку лимона чи навіть у синтезі ліків! Але що робить ці сполуки такими особливими? Відповідь криється в їхній функціональній групі, яка визначає їхні хімічні властивості та поведінку. Давайте розберемося, що це за група і чому вона настільки важлива.
Функціональна група – це специфічна комбінація атомів у молекулі, яка відповідає за її реакційну здатність. У карбонових кислот вона є серцем молекули, надаючи їй унікальні характеристики, такі як кислотність чи здатність утворювати складні ефіри. Але про все по порядку!
Функціональна група карбонових кислот: детальний погляд
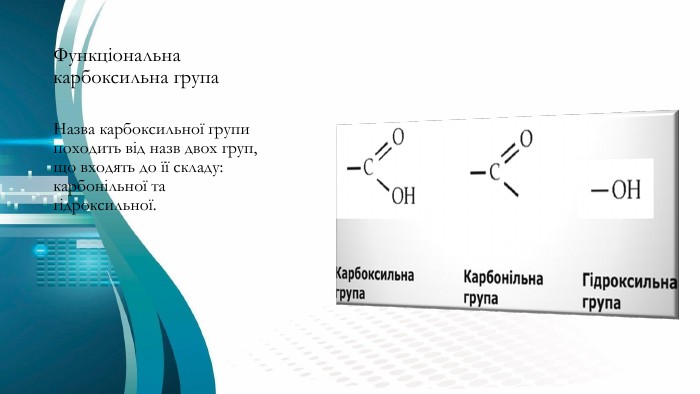
Карбонові кислоти мають функціональну групу, яка називається карбоксильною групою і позначається як -COOH. Ця група складається з карбонільного зв’язку (C=O) та гідроксильної групи (O-H), об’єднаних навколо одного атома вуглецю. Саме ця комбінація робить карбонові кислоти такими універсальними в органічній хімії.
Щоб зрозуміти, як це працює, уявіть карбоксильну групу як маленьку “хімічну фабрику”. Карбонільна частина (C=O) забезпечує високу реакційну здатність, а гідроксильна частина (O-H) дозволяє молекулі віддавати протон (H⁺), що й робить сполуку кислотною. Ця подвійна природа дозволяє карбоновим кислотам брати участь у найрізноманітніших реакціях – від утворення солей до створення складних органічних молекул.
Хімічна структура карбоксильної групи
Карбоксильна група виглядає так: R-COOH, де R – це залишок молекули (алкільна, арильна або інша органічна група). Наприклад, у оцтовій кислоті (CH₃COOH) R – це метильна група (CH₃). Ось як можна розкласти карбоксильну групу на складові:
- Карбонільна група (C=O): Подвійний зв’язок між вуглецем і киснем. Цей зв’язок надзвичайно міцний і поляризований, що робить вуглець частково позитивно зарядженим і привабливим для нуклеофілів.
- Гідроксильна група (O-H): Зв’язок між киснем і воднем, який легко розривається, дозволяючи молекулі проявляти кислотні властивості.
- Центральний атом вуглецю: Він тримає все разом, з’єднуючи R-групу, карбонільний кисень і гідроксильну групу.
Ця унікальна структура робить карбоксильну групу не лише реактивною, але й надзвичайно стабільною. Завдяки резонансу (електронному зміщенню між атомами кисню), карбоксильна група може розподіляти заряд, що знижує її енергію та підвищує стійкість молекули.
Чому карбоксильна група визначає властивості кислот
Карбоксильна група – це не просто набір атомів, а справжній “диригент” хімічних властивостей карбонових кислот. Вона впливає на їхню кислотність, розчинність і здатність вступати в реакції. Давайте розглянемо, як саме це відбувається.
Кислотність карбонових кислот
Карбонові кислоти є слабкими кислотами, але значно сильнішими, ніж спирти чи феноли. Чому? Усе через резонанс у карбоксильній групі. Коли кислота втрачає протон (H⁺), утворюється карбоксилат-іон (R-COO⁻), який стабілізується завдяки делокалізації негативного заряду між двома атомами кисню. Ця стабільність робить карбонові кислоти більш схильними до дисоціації у воді.
Для порівняння: оцтова кислота (CH₃COOH) має константу дисоціації (Kₐ) приблизно 1.8 × 10⁻⁵, що вказує на її слабку, але помітну кислотність. Сильніші кислоти, як мурашина (HCOOH), мають вищу Kₐ через менший розмір R-групи, що підсилює електронегативний ефект.
Розчинність у воді
Менші карбонові кисл оти, такі як мурашина чи оцтова, добре розчиняються у воді. Це пояснюється здатністю карбоксильної групи утворювати водневі зв’язки з молекулами води. Уявіть, як гідроксильна частина -COOH “чіпляється” за воду, створюючи міцні міжмолекулярні зв’язки. Однак із збільшенням довжини вуглецевого ланцюга (наприклад, у стеариновій кислоті C₁₇H₃₅COOH) розчинність зменшується, адже гідрофобний “хвіст” починає домінувати.
Реакційна здатність
Карбоксильна група робить кислоти надзвичайно універсальними в реакціях. Ось кілька прикладів, які демонструють її багатогранність:
- Утворення солей: Карбонові кислоти реагують із основами, утворюючи солі. Наприклад, оцтова кислота з гідроксидом натрію дає ацетат натрію (CH₃COONa).
- Естерифікація: Реакція з спиртами за наявності каталізатора утворює ефіри, які використовуються в парфумерії та харчовій промисловості.
- Відновлення: Карбонові кислоти можна відновити до спиртів, хоча це вимагає сильних відновників, як-от літій алюміній гідрид (LiAlH₄).
Ці реакції – лише вершина айсберга. Карбоксильна група відкриває двері до синтезу складних молекул, від ліків до полімерів. Наприклад, за даними підручника “Organic Chemistry” Джона МакМюррі (2023), карбонові кислоти є основою для синтезу аспірину, де саліцилова кислота модифікується через естерифікацію.
Порівняння карбонових кислот з іншими класами сполук
Щоб краще зрозуміти унікальність карбоксильної групи, порівняймо карбонові кислоти з іншими органічними сполуками. Таблиця нижче допоможе розібратися в ключових відмінностях.
| Клас сполук | Функціональна група | Кислотність | Типові реакції |
|---|---|---|---|
| Карбонові кислоти | -COOH | Слабка (Kₐ ~10⁻⁴–10⁻⁵) | Естерифікація, утворення солей |
| Спирти | -OH | Дуже слабка (Kₐ ~10⁻¹⁶) | Окиснення, дегідратація |
| Альдегіди | -CHO | Не кислотні | Окиснення до кислот |
Джерело: адаптовано з “Chemistry: The Central Science” Брауна та ін. (2022).
Як бачимо, карбоксильна група робить карбонові кислоти унікальними завдяки своїй кислотності та різноманітності реакцій. На відміну від спиртів, які мають лише гідроксильну групу, карбонові кислоти поєднують у собі силу карбонільного та гідроксильного компонентів.
Цікаві факти по темі
Карбонові кислоти всюди! Чи знали ви, що мурашина кислота (HCOOH) – це секрет пекучого укусу мурах? Її назва походить від латинського “formica” (мураха). 🐜
Оцтова кислота – не лише основа оцту, а й ключовий компонент у виробництві пластику, як-от полівінілацетату.
Жирні кислоти, такі як стеаринова чи олеїнова, є карбоновими кислотами, які формують основу наших клітинних мембран. Без них життя було б неможливим!
Бензойна кислота використовується як консервант у їжі (E210). Наступного разу, коли їстимете джем, згадайте про карбоксильну групу!
Ці факти лише підкреслюють, наскільки карбонові кислоти проникли в наше життя – від природи до промисловості. Їхня універсальність вражає, чи не так?
Як карбоксильна група впливає на номенклатуру
Назви карбонових кислот тісно пов’язані з їхньою структурою. За систематичною номенклатурою IUPAC карбоксильна група завжди має найвищий пріоритет, а вуглецевий атом -COOH вважається першим у ланцюзі. Наприклад:
- Мурашина кислота (HCOOH): Найпростіша карбонова кислота, де R – лише атом водню.
- Оцтова кислота (CH₃COOH): Два вуглеці в ланцюзі, тому назва походить від “етан”, але з суфіксом “-ова кислота”.
- Бутанова кислота (C₃H₇COOH): Чотири вуглеці, звідки й назва “бутанова”.
Цікаво, що багато карбонових кислот мають тривіальні назви, які походять із природи. Наприклад, мурашина кислота названа через мурах, а валеріанова – через валеріановий корінь. Це додає хімії трохи романтики, чи не так?
Застосування карбонових кислот у житті
Карбонові кислоти – це не лише абстрактні молекули з підручників. Вони всюди! Ось кілька сфер, де вони відіграють ключову роль:
- Харчова промисловість: Оцтова кислота використовується в оцті, а сорбінова кислота – як консервант у хлібі та сирах.
- Фармацевтика: Ацетилсаліцилова кислота – це аспірин, який рятує від болю та запалень.
- Косметика: Жирні кислоти, як-от лауринова, є основою мила та кремів.
- Промисловість: Карбонові кислоти використовуються для виробництва полімерів, барвників і навіть біопалива.
Завдяки карбоксильній групі ці сполуки можуть адаптуватися до найрізноманітніших завдань. Їхня здатність утворювати водневі зв’язки та вступати в реакції робить їх незамінними в сучасному світі.
Типові помилки при вивченні карбонових кислот
Карбонові кислоти здаються простими, але студенти часто припускаються помилок, коли намагаються розібратися в їхніх властивостях. Ось кілька поширених пасток:
- Плутанина з іншими групами: Багато хто плутає карбоксильну групу (-COOH) з карбонільною (-CHO) чи гідроксильною (-OH). Пам’ятайте: лише -COOH робить сполуку кислотою!
- Неправильне розуміння кислотності: Карбонові кислоти – не сильні кислоти, як соляна (HCl). Їхня слабка кислотність зумовлена резонансною стабілізацією.
- Ігнорування резонансу: Резонанс у карбоксилат-іоні – ключ до розуміння їхньої поведінки. Без цього важко пояснити, чому вони такі активні.
Щоб уникнути цих помилок, завжди звертайте увагу на структуру карбоксильної групи та її унікальні властивості. Це допоможе вам не лише в навчанні, а й у практичному застосуванні знань.