Калій гідроксид (KOH), відомий як їдкий калій, — це хімічна зірка, що сяє своєю активністю в лабораторіях і промислових цехах. Як сильний луг, він вступає в реакції з безліччю речовин, створюючи нові сполуки, виділяючи тепло чи навіть змінюючи властивості матеріалів. У цій статті ми зануримося в захоплюючий світ хімічних взаємодій KOH, розкриваючи деталі, приклади та цікаві нюанси, які зроблять тему зрозумілою як для новачків, так і для досвідчених хіміків.
Хімічна природа калій гідроксиду: чому він такий реактивний?
Калій гідроксид — неорганічна сполука, що належить до гідроксидів лужних металів. Його формула KOH приховує потужну здатність віддавати гідроксид-іони (OH⁻), які й роблять його сильною основою. У воді KOH повністю дисоціює, створюючи сильно лужне середовище з pH до 13,5. Ця властивість дозволяє йому реагувати з кислотами, солями, оксидами, металами і навіть органічними сполуками.
Чому KOH такий активний? Його реактивність пояснюється високою електронегативністю гідроксид-іонів і низькою енергією іонізації калію, що полегшує хімічні взаємодії. Ця сполука, наче невтомний танцюрист, легко знаходить партнера для реакції, будь то кислота чи амфотерний гідроксид.
Реакції з кислотами: нейтралізація з видовищним ефектом
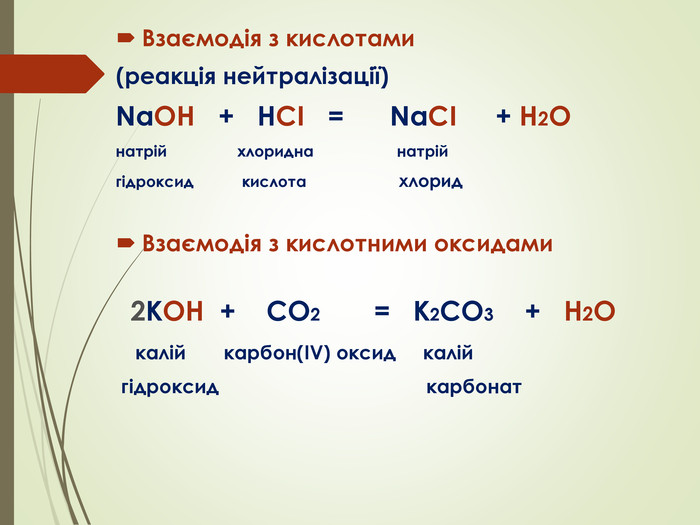
Одна з найпоширеніших реакцій калій гідроксиду — взаємодія з кислотами, що називається нейтралізацією. У результаті утворюються сіль і вода, а реакція часто супроводжується виділенням тепла.
Приклади реакцій з кислотами
Калій гідроксид реагує з різними кислотами, від простих до складних. Ось кілька прикладів:
- З соляною кислотою (HCl): KOH + HCl → KCl + H₂O. Утворюється хлорид калію, який використовують у добривах.
- З сірчаною кислотою (H₂SO₄): 2KOH + H₂SO₄ → K₂SO₄ + 2H₂O. Сульфат калію — цінний компонент у сільському господарстві.
- З азотною кислотою (HNO₃): KOH + HNO₃ → KNO₃ + H₂O. Нітрат калію застосовують у виробництві пороху.
Ці реакції — класика хімічної лабораторії. Вони не лише демонструють силу KOH як лугу, а й показують його практичне значення. Наприклад, нейтралізація кислот у промислових стоках за допомогою KOH допомагає очищати воду від шкідливих домішок.
Взаємодія з кислими оксидами: поглинання газів
Калій гідроксид активно реагує з кислими оксидами, такими як вуглекислий газ (CO₂) чи сірчистий газ (SO₂). Ці реакції важливі для очищення газів у промислових процесах.
Реакція з CO₂
При контакті з вуглекислим газом KOH утворює карбонат або гідрокарбонат калію залежно від умов:
- Утворення карбонату: 2KOH + CO₂ → K₂CO₃ + H₂O.
- Утворення гідрокарбонату: KOH + CO₂ → KHCO₃.
Ця властивість робить KOH незамінним у системах поглинання CO₂, наприклад, у підводних човнах чи космічних апаратах, де він очищає повітря від надлишку вуглекислого газу.
Реакції з амфотерними речовинами: унікальна хімія
Калій гідроксид здатен реагувати з амфотерними оксидами та гідроксидами, такими як оксид алюмінію (Al₂O₃) чи гідроксид цинку (Zn(OH)₂). Це дозволяє отримувати комплексні сполуки.
Приклади амфотерних реакцій
Ось як KOH взаємодіє з амфотерними речовинами:
- З гідроксидом алюмінію: Al(OH)₃ + KOH → KAlO₂ + 2H₂O (у розчині) або 2Al(OH)₃ + 3KOH → K₃AlO₃ + 6H₂O (при сплавленні).
- З гідроксидом цинку: Zn(OH)₂ + 2KOH → K₂Zn(OH)₄ (цинкат калію).
Такі реакції демонструють унікальну здатність KOH взаємодіяти з речовинами, які проявляють як кислотні, так і основні властивості. Вони широко застосовуються у виробництві алюмінатів і цинкатів.
Реакції з солями та металами
Калій гідроксид може вступати в реакції обміну з солями, якщо утворюється нерозчинна сполука або слабкий електроліт. Також він реагує з деякими металами, особливо в умовах високих температур.
Реакція з солями
Приклад: KOH реагує з хлоридом заліза(III):
FeCl₃ + 3KOH → Fe(OH)₃↓ + 3KCl.
Утворюється нерозчинний гідроксид заліза(III), який випадає в осад. Ця реакція використовується в аналітичній хімії для виявлення іонів заліза.
Реакція з металами
При високих температурах KOH реагує з алюмінієм:
2Al + 2KOH + 6H₂O → 2KAl(OH)₄ + 3H₂↑.
Ця реакція супроводжується виділенням водню, що робить її потенційно небезпечною, але корисною для лабораторних експериментів.
Органічні реакції: KOH у світі вуглеводнів
Калій гідроксид також грає важливу роль в органічній хімії. Він реагує з органічними кислотами, алкінами та іншими сполуками, що мають кислотні властивості.
Реакція з карбоновими кислотами
Наприклад, з оцтовою кислотою:
CH₃COOH + KOH → CH₃COOK + H₂O.
Утворюється ацетат калію, який використовують у виробництві мила та інших продуктів.
Виробництво мила
Одне з найвідоміших застосувань KOH — омилення жирів. У реакції з тригліцеридами (жирами) утворюються гліцерин і калійні солі жирних кислот (мило):
C₃H₅(OCOR)₃ + 3KOH → C₃H₅(OH)₃ + 3RCOOK.
Цей процес лежить в основі виробництва рідкого мила, яке цінується за м’якість і розчинність.
Реакції з галогенами та пероксидами
Калій гідроксид може реагувати з галогенами (наприклад, хлором) або пероксидами, утворюючи солі чи пероксид калію.
Реакція з хлором
При пропусканні хлору через розчин KOH за низьких температур утворюються хлорид і гіпохлорит калію:
2KOH + Cl₂ → KCl + KClO + H₂O.
За високих температур може утворитися хлорат калію (KClO₃), який використовують у піротехніці.
Реакція з пероксидом водню
При взаємодії з H₂O₂ утворюється пероксид калію:
2KOH + H₂O₂ → K₂O₂ + 2H₂O.
Ця реакція вимагає подальшої дегідратації для отримання чистого K₂O₂.
Практичне застосування реакцій KOH
Реакції калій гідроксиду знаходять застосування в багатьох галузях. Ось основні з них:
- Виробництво мила та косметики: Омилення жирів для рідкого мила та стеаринових емульсій.
- Хімічна промисловість: Виробництво карбонатів, нітратів, перманганатів.
- Очищення: Поглинання CO₂ і SO₂ у газоочисних системах.
- Енергетика: Використання як електроліту в лужних акумуляторах.
Кожна з цих галузей залежить від унікальних хімічних властивостей KOH, що робить його незамінним у сучасному світі.
Цікаві факти про калій гідроксид
Калій гідроксид — це не лише хімічна сполука, а й речовина з багатою історією та несподіваними застосуваннями. Ось кілька захоплюючих фактів:
- 🌱 Старовинне миловаріння: У минулому KOH отримували з деревної золи, змішуючи її з вапном, що дозволяло створювати м’яке калійне мило.
- 🚀 Космічні технології: KOH використовують у системах регенерації повітря на космічних станціях, поглинаючи CO₂.
- ⚡ Енергія майбутнього: У лужних батареях KOH забезпечує високу провідність, що робить їх ефективними для гібридних автомобілів, як-от Toyota Prius.
- 🍫 Харчова промисловість: Як добавка E525, KOH регулює кислотність у виробництві шоколаду та какао.
Ці факти показують, наскільки багатогранним є калій гідроксид, виходячи за межі лабораторних стін.
Таблиця: Основні реакції калій гідроксиду
Для зручності ми зібрали ключові реакції KOH у таблиці:
| Тип речовини | Приклад реакції | Продукти | Застосування |
|---|---|---|---|
| Кислота | KOH + HCl → KCl + H₂O | Хлорид калію, вода | Добрива |
| Кислий оксид | 2KOH + CO₂ → K₂CO₃ + H₂O | Карбонат калію, вода | Очищення газів |
| Амфотерний гідроксид | Zn(OH)₂ + 2KOH → K₂Zn(OH)₄ | Цинкат калію | Хімічний синтез |
| Органічна кислота | CH₃COOH + KOH → CH₃COOK + H₂O | Ацетат калію, вода | Виробництво мила |
Джерела: uk.wikipedia.org, en.wikipedia.org.
Безпека при роботі з KOH
Калій гідроксид — потужна, але небезпечна речовина, що може викликати опіки шкіри та слизових.
При роботі з KOH необхідно використовувати захисні рукавички, окуляри та працювати в добре вентильованому приміщенні. У разі потрапляння на шкіру промийте уражену ділянку розчином оцтової чи лимонної кислоти, а потім водою. Ці заходи безпеки допоможуть уникнути неприємних наслідків.
Чому KOH такий важливий для хімії та промисловості?
Калій гідроксид — це не просто хімічна сполука, а справжній каталізатор прогресу. Його реакції лежать в основі багатьох процесів, від створення мила до очищення повітря в космосі. Завдяки своїй універсальності KOH залишається незамінним у лабораторіях, на заводах і навіть у побуті.
Розуміння того, з якими речовинами реагує калій гідроксид, відкриває двері до безлічі практичних застосувань. Ця сполука, наче чарівна паличка, перетворює сировину на корисні продукти, роблячи наше життя комфортнішим і безпечнішим.